ENFERMEDAD HEMOLÍTICA DEL RECIÉN NACIDO
FISIOPATOLOGÍA
La hemólisis por anticuerpos anti Rh fue —y sigue siendo— la principal causa de enfermedad hemolítica severa del recién nacido, pero, además, existen otros anticuerpos aloinmunes de Kell (K y k), Duffy (Fya), Kidd (Jka y Jkb) y MNSs (M, N, S y s) que también son causa de enfermedad hemolítica.
El sistema del grupo sanguíneo Rhesus (Rh) que usa la nomenclatura Fisher-Race, y el complejo del gen, consta de 3 loci (posición cromosómica de varios genes) genéticos cada uno con 2 alelos (genes que se ubican en el mismo sitio en cromosomas homólogos) principales. Codifican éstos para 5 antígenos principales identificados con letras C, c, E, e y D. Los antígenos del grupo sanguíneo Rh se heredan según lo determinan al menos 2 proteínas homólogas, pero distintas asociadas a la membrana. Dos genes separados (RhCE y RhD) localizados en el brazo corto del cromosoma 1 (1p36-p34), codifican las proteínas Rh. Cada gen tiene una longitud de 10 exones y se observa homología en 96% de los genes.
Grupo Rh
Los genes que codifican el grupo Rh son complejos y altamente polimórficos. Los dos genes previamente mencionados RhD y RhCE, que están estrechamente relacionados, han sufrido numerosos reordenamientos produciendo genes Rh híbridos que codifican un gran número de antígenos distintos; se conocen aproximadamente 49 diferentes. Por lo anterior, los antígenos Rh son altamente inmunogénicos y se explicará su mecanismo patológico a continuación como ejemplo de los demás tipos de incompatibilidad, ya que es el principal.
Isoinmunización materna
El proceso de isoinmunización materna se lleva a cabo de manera escalonada con antecedentes necesarios para su realización. En el caso de una mujer con grupo sanguíneo Rh negativo gestante de un feto que, por herencia, es portador del grupo sanguíneo del padre (en mayor frecuencia RhD para el ejemplo, también puede ser del grupo ABO), son ajenos al sistema inmunológico materno, en el momento en que la sangre fetal entra en contacto con la circulación materna, ya sea durante el último trimestre del embarazo, cuando el citotrofoblasto ya no está presente, o durante el parto, puede sensibilizarse, esto ocurre en la primera exposición materna al grupo Rh positivo (Rh+), que usualmente es durante el primer embarazo.
La cantidad necesaria de sangre fetal que puede desencadenar incompatibilidad varía, se ha demostrado que menos de 1ml de sangre Rh+ podría causar sensibilización; en el 90% de los casos, dicha sensibilización ocurre durante el parto, por lo anterior, la mayoría de los primogénitos Rh+ de madres Rh- no se ven afectados por el corto periodo desde la primera exposición de eritrocitos fetales. Un mes después, una vez que ocurre la sensibilización, la madre crea anticuerpos IgG anti-Rh, mismos que siempre pueden pasar la barrera placentaria.
El riesgo de sensibilización materna depende en gran medida de los siguientes 3 factores:
• Volumen de hemorragia trasplacentaria
• Alcance de la respuesta inmune materna (tiempo de exposición del feto a la respuesta inmune materna)
• Presencia concurrente de incompatibilidad ABO o cualquier otra.
Con cada embarazo de una madre sensibilizada, el riesgo y la gravedad de la respuesta inmune aumentan, desde un recién nacido anémico, hasta un feto muerto de forma intrauterina por la reacción a la anemia hemolítica inducida por la respuesta inmune masiva.

Feto
Una madre ya sensibilizada con anticuerpos propios IgG anti-Rh, al pasar de la madre al feto vía placentaria, generan una reacción de hemólisis contra los eritrocitos fetales, causando una serie de consecuencias mencionadas a continuación:
• Hematopoyesis extramedular en hígado y bazo secundaria a la anemia fetal
• Eventualmente, cuando la anemia no logre compensarse y los eritrocitos no sean suficientes para la demanda oxigénica, el corazón y el hígado (principalmente) sufren una lesión hipóxica provocando una insuficiencia circulatoria y hepática.
• La síntesis de proteínas hepáticas disminuye secundario a la falla, lo cual genera una reducción en la presión oncótica de la circulación fetal.
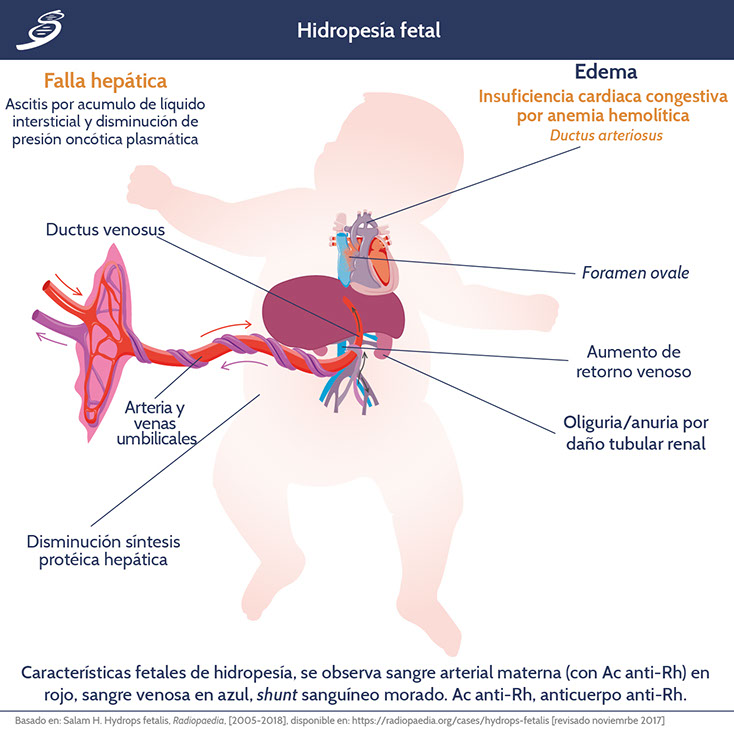
• La hipoxia crónica y falla hepática generan insuficiencia cardiaca provocando un aumento en la presión venosa, la cual aumenta el daño hepático y genera edema y ascitis hasta la hidropesía fetal (hydrops fetalis).
Hidropesía fetal
El desequilibrio generado en el líquido intersticial y retorno linfático por la insuficiencia cardiaca congestiva y la disminución en la presión oncótica, llevan a la acumulación de líquido intersticial debido a la mayor permeabilidad capilar fetal. Existen mecanismos compensatorios que se llevan a cabo para mantener la homeostasis durante la hipoxia para mayor eficacia de la extracción de oxígeno deficiente, uno de ellos es la redistribución del flujo sanguíneo que favorece cerebro, corazón y glándulas suprarrenales, llegando a causar daño tubular renal; otro mecanismo es el aumento del volumen para mejorar el gasto cardiaco y una marcada activación del sistema renina-angiotensina.
A pesar de los esfuerzos, los mismos mecanismos compensatorios aumentan también la presión venosa incrementando aún más la acumulación de líquido intersticial y generando cambios hidropónicos característicos morfológicamente del feto. La alteración generada de la función renal causa oliguria o anuria hasta, posteriormente, hidropesía.
Recién nacido
En el recién nacido, el principal síntoma de la anemia hemolítica es la aparición de ictericia, lo cual ocurre dentro de las siguientes 24 hrs del nacimiento. Dependiendo del grado de la anemia en el neonato, puede haber, además: palidez, hepatoesplenomegalia hasta incluso hidropesía. La aparición de ictericia es secundaria a la destrucción eritrocitaria y del grupo hemo, generando una acumulación de la bilirrubina indirecta y pudiendo llegar a niveles tóxicos para el sistema nervioso que genera una condición llamada kernicterus, esto se clasifica de acuerdo a la cuenta de bilirrubinas directas, indirectas, totales, grado de anemia, edad gestacional y peso. Sin tratamiento, esto puede llegar a ser fatal o dejar secuelas muy graves para la vida y el correcto funcionamiento del cuerpo.
Bibliografía
1,. Salem L. Rh Incompatibility, Emergency Medicine, [Updated: Mar 15, 2017] disponible en: https://emedicine.medscape.com/article/797150-overview#a5 [revisado noviembre 2017]
2. Wagle S. Hemolytic Disease of Newborn, Pediatrics: Cardiac Disease and Critical Care Medicine, [Updated: Jan 02, 2016] disponible en: https://emedicine.medscape.com/article/974349-overview#a5 [revisado noviembre 2017]
3. Dean L. Blood Groups and Red Cell Antigens [Internet]. Bethesda (MD): National Center for Biotechnology Information (US); 2005.
4. Krafts K. Hemolytic disease of the newborn, Pathology Student, [Sep 25, 2009] disponible en: http://www.pathologystudent.com/?p=1521 [revisado noviembre 2017]
5. Bellini C, Hennekam RC. Non-immune hydrops fetalis: a short review of etiology and pathophysiology, Am J Med Genet A, 2012; 158 (3):597-605.
6. ULLAH S, RAHMAN K y HEDAYATI M. Hyperbilirubinemia in Neonates: Types, Causes, Clinical Examinations, Preventive Measures and Treatments: A Narrative Review Article, Iran J Public Health, 2016; 45(5): 558–568.
7. Roopenian DC, Akilesh S. FcRn: the neonatal Fc receptor comes of age, Nat Rev Immunol, 2007; 7(9):715-25
Enciclopedia Británica. Erythroblastosis fetalis, PATHOLOGY, [2017], disponible en: https://www.britannica.com/science/erythroblastosis-fetalis#ref922141 [revisado noviembre 2017]
8. Salam H. Hydrops fetalis, Radiopaedia, [2005-2018], disponible en: https://radiopaedia.org/cases/hydrops-fetalis [revisado noviemrbe 2017]
Periodismo científico cultural
Sobre el cigarro electrónico
Ya ha pasado tiempo desde que el cigarro se convirtió en el enemigo público número uno, tanto para fumadores como para no fumadores...
[leer mas]
la sal! Tu cerebro
y corazón lo agradecerán
La enfermedad diverticular y sus complicaciones son una causa importante de morbimortalidad en todo el mundo...
[leer mas]
El primer anticuerpo monoclonal para pacientes con hemofilia A e inhibidores a FVIII
Cuando se vive con hemofilia todo puede ser una amenaza para provocar sangrados; desde niños...
[leer mas]
Infografías
TODOS LOS DERECHOS RESERVADOS © SPG COMUNICACIONES SA DE CV 2012-2018
Diseño: A. Victoria Pérez
Aviso de privacidad




